
SI-BONE, Inc. anuncia los resultados de dos años de un ensayo controlado aleatorio del iFuse Implant System®
- SI-BONE, Inc. anuncia los resultados de dos años de un ensayo controlado aleatorio del iFuse Implant System® frente al tratamiento no quirúrgico de algunas causas de disfunción de articulación sacroilíaca
El RCT de dos años demuestra la duración a largo plazo de iFuse, validando más los resultados anteriores publicados de 3, 4 y 5 años
SAN JOSÉ, California, 5 de septiembre de 2016 /PRNewswire/ -- SI-BONE, Inc., una compañía de dispositivos médicos pionera en el uso del iFuse Implant System® ("iFuse"), un dispositivo quirúrgico mínimamente invasivo (MIS) de forma triangular indicado para la fusión para determinados desórdenes de la articulación sacroiliaca (SI), anunció hoy la publicación de los resultados de dos años de INSITE (Investigation of Sacroiliac Fusion Treatment - NCT01681004), un ensayo controlado aleatorio, multicentro y prospectivo (RCT) de la fusión MIS de articulación SI con iFuse en comparación con el tratamiento no quirúrgico (NSM). Los resultados de este estudio de alta calidad de nivel 1 se publicaron en International Journal of Spine Surgery con el título: Two-Year Outcomes from a Randomized Controlled Trial of Minimally Invasive Sacroiliac Joint Fusion vs. Non-Surgical Management for Sacroiliac Joint Dysfunction1. El estudio demostró que las mejoras rápidas en el dolor, discapacidad y calidad de vida en el grupo iFuse fueron superiores a las vistas en el grupo NSM, siendo duraderas hasta dos años. Este amplio RCT de nivel1 se añade a las más de 40 publicaciones revisadas sobre iFuse, reforzando más los resultados positivos y duración del producto demostrada en las anteriores publicaciones de 3, 4,5 y 5 años.2-4
Foto - http://photos.prnewswire.com/prnh/20160823/400554
Foto - http://photos.prnewswire.com/prnh/20160823/400553
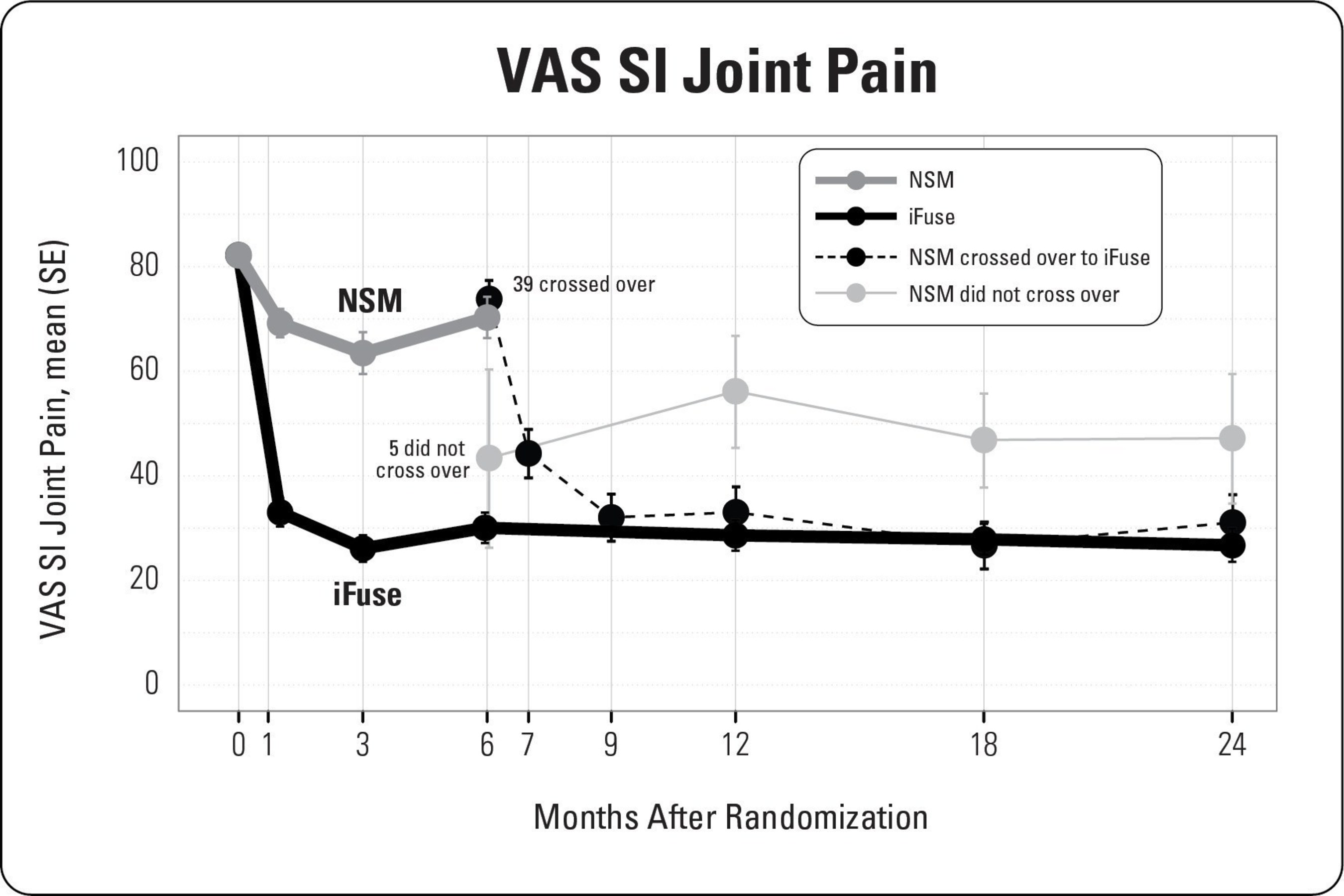
Se reclutaron 148 sujetos, de forma aleatoria 2:1 (102 iFuse/46 NSM), y bajo tratamiento en 19 centros en Estados Unidos, incluyendo ambas prácticas, privadas e instituciones académicas. En el grupo iFuse, la puntuación media de dolor de la articulación SI mejoró desde los 82,3 en la línea de base hasta los 30,1 a los 6 meses, 28,6 a los 12 meses y 26,7 a los dos años, correspondiente a las mejoras desde la línea base de 52,3, 53,7 y 55,4 puntos, respectivamente (todos p<.0001, figura 1). La discapacidad, evaluada usando el Oswestry Disability Index (ODI), se redujo desde una media de 57,2 en la línea base hasta los 29,9, 28,3 y 28,7 a los 6, 12 y 24 meses, lo que representa una mejora media de 27,4, 28,9 y 28,4 puntos, respectivamente (p<.0001)
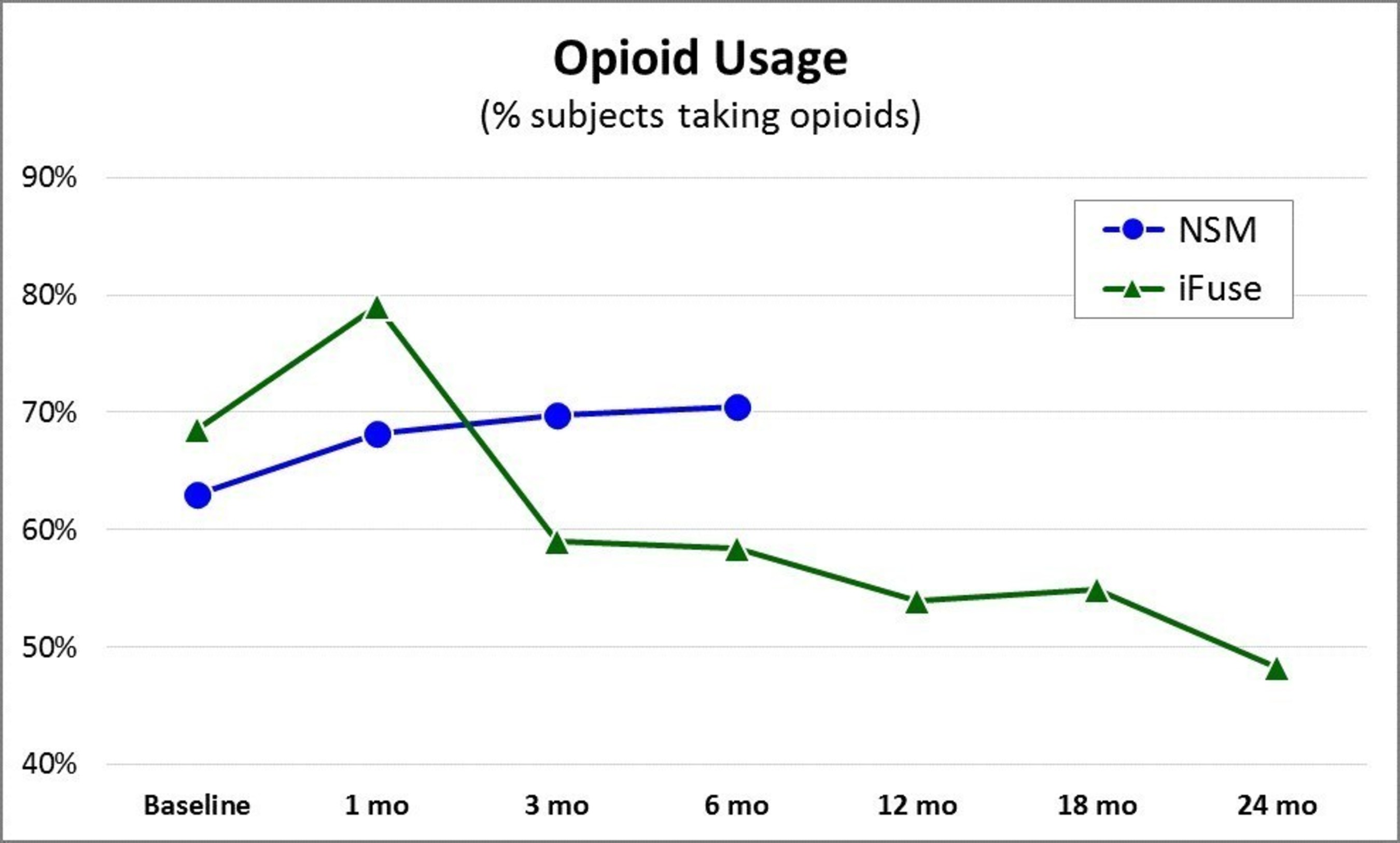
La tasa de revisión de cirugía fue tan baja como de un 3,4% (3/89), siendo consistente con los resultados de largo plazo indicados anteriormente para iFuse2,5 y aproximadamente de la tercera parte para la cirugía de fusión lumbar6. Los resultados de dos años demostraron además un descenso de un 29,7% desde la línea base en la cifra de sujetos del estudio que tomaban opioides (figura 2), siendo consistente con la reducción de un 28% en el uso de opioides observado en un estudio multicentro prospectivo de dos años indicado con anterioridad5.
"Estos resultados de dos años del estudio INSITE ilustran la duración de la fusión de articulación SI con iFuse y validan los resultados indicados anteriormente de 6 y 12 meses que mostraron una mejora rápida del dolor, función y calidad de vida dentro de esta población de pacientes altamente debilitada", explicó Frank Phillips, MD del Rush University Medial Center de Chicago, IL. "Esta publicación positiva valida la consistencia de las publicaciones anteriores sobre iFuse, y esperamos sirva para instar los planes de salud en Estados Unidos de cara a la cobertura de este procedimiento eficaz".
Acerca de SI-BONE, Inc.SI-BONE, Inc. (San José, California) es una compañía de dispositivos médicos de articulaciones sacroilíacas líder dedicada al desarrollo de herramientas y productos para diagnosticar y tratar a los pacientes que padecen dolores lumbares de espalda relacionados con algunas enfermedades de las articulaciones SI. La compañía desarrolla, fabrica y comercializa productos mínimamente invasivos para la articulación SI. SI-BONE, Inc. recibió el permiso original 510(k) en noviembre de 2008 a través de la Administración de Fármacos y Alimentos (FDA) para comercializar el iFuse Implant System. La Marca CE para la comercialización en Europa se consiguió en noviembre de 2010.
El iFuse Implant System es una opción quirúrgica mínimamente invasiva que utiliza implantes de titanio recubiertos por una superficie porosa que actúa como una superficie de interferencia, diseñada para ayudar a reducir el movimiento del implante, y permitir la fusión biológica para apoyar la fijación a largo plazo. iFuse es el único dispositivo de fusión de la articulación SI en Estados Unidos con evidencia publicada que demuestra la seguridad, efectividad y beneficios económicos, que incluyen tres estudios prospectivos multicentro, dos de los cuales son ensayos controlados aleatorios (RCTs). Actualmente, hay más de 40 publicaciones revisadas por pares que apoyan los resultados clínicos positivos, seguridad, biomecánica y el valor económico de iFuse. Es el único producto de fusión de la articulación SI con una aprobación de la FDA reconociendo que los estudios clínicos demuestran mejora en el dolor, función del paciente y calidad de vida.
El iFuse Implant System está orientado a la fusión de la articulación sacroilíaca para condiciones que incluyen la disfunción de la articulación SI que es un resultado directo de las disrupciones de la articulación SI y la sacroilitis degenerativa. Estas incluyen condiciones cuyos síntomas comiencen durante el embarazo o en el periodo de periparto y que persisten post-parto durante más de seis meses. Estudios clínicos han demostrado que el tratamiento con el iFuse Implant System mejora el dolor, función del paciente y calidad de vida. Hay riesgos potenciales asociados al iFuse Implant System. Puede no ser adecuado para todos los pacientes y todos los pacientes podrían no beneficiarse de ello. Si desea más información sobre los riesgos visite: www.si-bone.com/risks
SI-BONE e iFuse Implant System son marcas registradas de SI-BONE, Inc. ©2016 SI-BONE, Inc. Todos los derechos reservados. 9695.082416
- Polly DW, Swofford J, Whang PG, Frank CJ, Glaser JA, Limoni RP, Cher DJ, Wine KD, Sembrano JN, and the INSITE Study Group. Two-Year Outcomes from a Randomized Controlled Trial of Minimally Invasive Sacroiliac Joint Fusion vs. Non-Surgical Management for Sacroiliac Joint Dysfunction. Int J Spine Surg. 2016;10:Article 28. doi: 10.14444/3028.
- Sachs D, Kovalsky D, Redmond A, Limoni R, Meyer SC, Harvey C, Kondrashov D. Durable Intermediate- to Long-term Outcomes after Minimally Invasive Transiliac Sacroiliac Joint Fusion using Triangular Titanium Implants. Med Devices (Auckl). 2016;9:213-22. doi: 10.2147/MDER.S109267.
- Vanaclocha-Vanaclocha V, Verdú-López F, Sánchez-Pardo M, Gozalbes-Esterelles L, Herrera JM, Rivera-Paz M, Martínez-Gómez D. Minimally Invasive Sacroiliac Joint Arthrodesis: Experience in a Prospective Series with 24 Patients. J Spine. 2014;3:185. doi: 10.4172/2165-7939.1000185.
- Rudolf L, Capobianco R. Five-Year Clinical and Radiographic Outcomes After Minimally Invasive Sacroiliac Joint Fusion Using Triangular Implants. Open Orthop J. 2014;8:375–83. doi: 10.2174/1874325001408010375.
- Duhon BS, Bitan F, Lockstadt H, Kovalsky DA, Cher DJ, Hillen T, on behalf of the SIFI Study Group. Triangular Titanium Implants for Minimally Invasive Sacroiliac Joint Fusion: 2-year Follow-up from a Prospective Multicenter Trial. Int J Spine Surg. 2016;10:Article 13. doi: 10.14444/3013.
- Martin BI, Mirza SK, Comstock BA, Gray DT, Kreuter W, Deyo RA. Reoperation rates following lumbar spine surgery and the influence of spinal fusion procedures. Spine. 2007;32(3):382-7. doi: 10.1097/01.brs.0000254104.55716.46.
Una o más de las personas a las que se hace referencia podría ser o haber sido empleado de SI-BONE, consultor de pago, inversor, investigador de pruebas médicas o receptor de una beca. La investigación a la que se hace referencia recibió el apoyo de SI-BONE.

Share this article